機能性表示食品制度於 2015 年施行,與特定保健用食品(特保)不同,不需消費者廳個別承認、僅需申報。事業者依科學根據自負其責標示機能,是中小品牌與原料商也能運用的制度。
但「僅需申報」這四個字若鬆懈會吃虧。申報資料實質受審查,不齊全則退件,最壞會被撤回勸告。本文介紹真鶴薬事組日常運轉的 申報實務流程。
01制度全貌
機能性表示食品需以申報書呈現五要素:(1) 機能性關連成分特定、(2) 安全性科學根據、(3) 機能性科學根據、(4) 製造/品質管理、(5) 標示見本。資料整備通常需 6〜12 個月。
02原料選定:3 條路徑
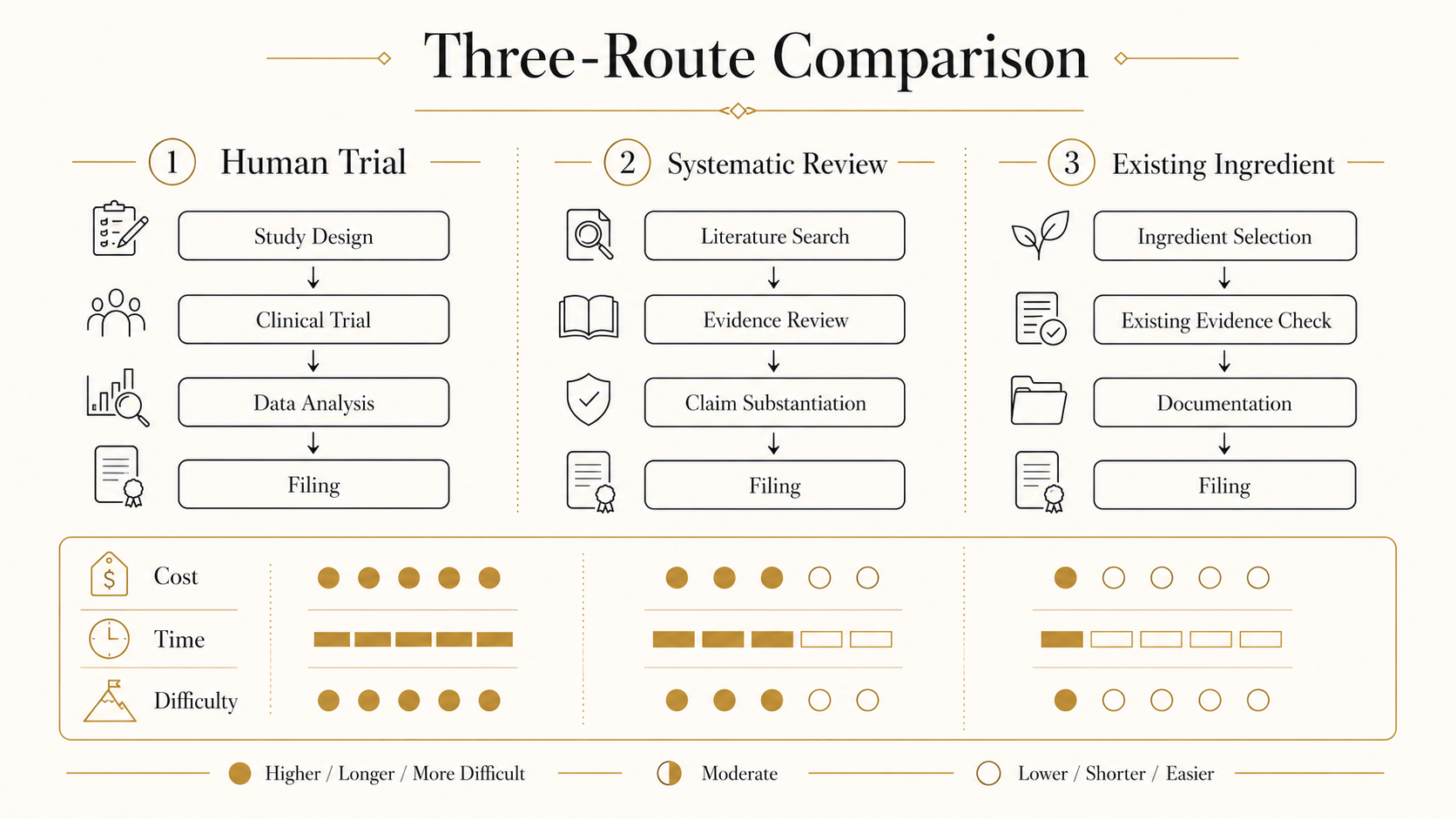
機能性根據建構方法:(A) 最終商品人體試驗、(B) 機能性關連成分研究回顧、(C) 既有申報原料使用。中小品牌建議 (C) → (B) 順序。使用已有申報實績的原料可大幅降低安全性評估負擔。
03研究回顧(系統性回顧)
研究回顧需從 PubMed、醫中誌、JDream III 等資料庫,依 PRISMA 準則 全面收集人體介入試驗並進行品質評估。需專業統計知識與論文判讀力,通常與外部委託機構協作。
- 檢索式建構(PICO 設計)
- 資料庫檢索與重複排除
- 論文篩選(一次/二次)
- 論文品質評估(Cochrane Risk of Bias)
- 定性/定量整合(meta-analysis)
- 回顧報告書撰寫
採用論文「數量」之外,「品質」更被重視。偏差風險高的試驗為主則機能性根據被認定薄弱。
04安全性評估
三層建構:(1) 既有資訊評估、(2) 攝取實績評估、(3) 安全性試驗實施。長年食用經驗的原料以 (1)(2) 構成;新原料需 (3) 毒性試驗。
05申報書結構
申報書由樣式 I〜VII 構成,附件包含研究回顧報告書、安全性評估書、製造工程流程圖、標示見本。總頁數約 200〜400 頁。

06送件與公告
透過消費者廳申報資料庫電子送件。受理後 60 日 內無退件則公告,可開始上架標示。退件時需撰寫回覆書並重送,初次申報 2〜3 次往返為正常。
「申報一次到位」是錯覺,「以兩次往返為前提排時程」是現場鐵律。— 真鶴 薬事組
真鶴從原料選定到申報代行一條龍承接。→ 聯絡我們
