機能性表示食品制度は、2015年に施行された比較的新しい食品表示制度です。特定保健用食品(トクホ)と異なり、消費者庁の 個別承認は不要・届出のみ。事業者が科学的根拠に基づいて自らの責任で機能性を表示できる仕組みで、中小ブランドや原料供給者にとっても活用可能な制度設計になっています。
ただし、「届出のみ」という言葉に油断すると痛い目を見ます。届出資料は実質的に審査の対象となり、不備があれば差戻し、最悪の場合は撤回勧告まであり得ます。本稿では、真鶴が薬事チームで日々動かしている 届出実務の段取り をお伝えします。
01制度の全体像
機能性表示食品は、(1) 機能性関与成分の特定、(2) 安全性の科学的根拠、(3) 機能性の科学的根拠、(4) 製造・品質管理、(5) 表示見本の5要素を届出書類で示すことで、機能性表示が可能になります。これらの整備に通常 6〜12ヶ月を要します。
02原料選定:3つの選択肢
機能性根拠の構築方法は、(A) 最終製品でのヒト試験、(B) 機能性関与成分の研究レビュー、(C) 既存届出原料の使用の3つ。中小ブランドが最初に取るべきルートは (C) → (B)の順です。すでに届出実績のある原料を使用すれば、安全性評価の負担が大幅に軽減されます。
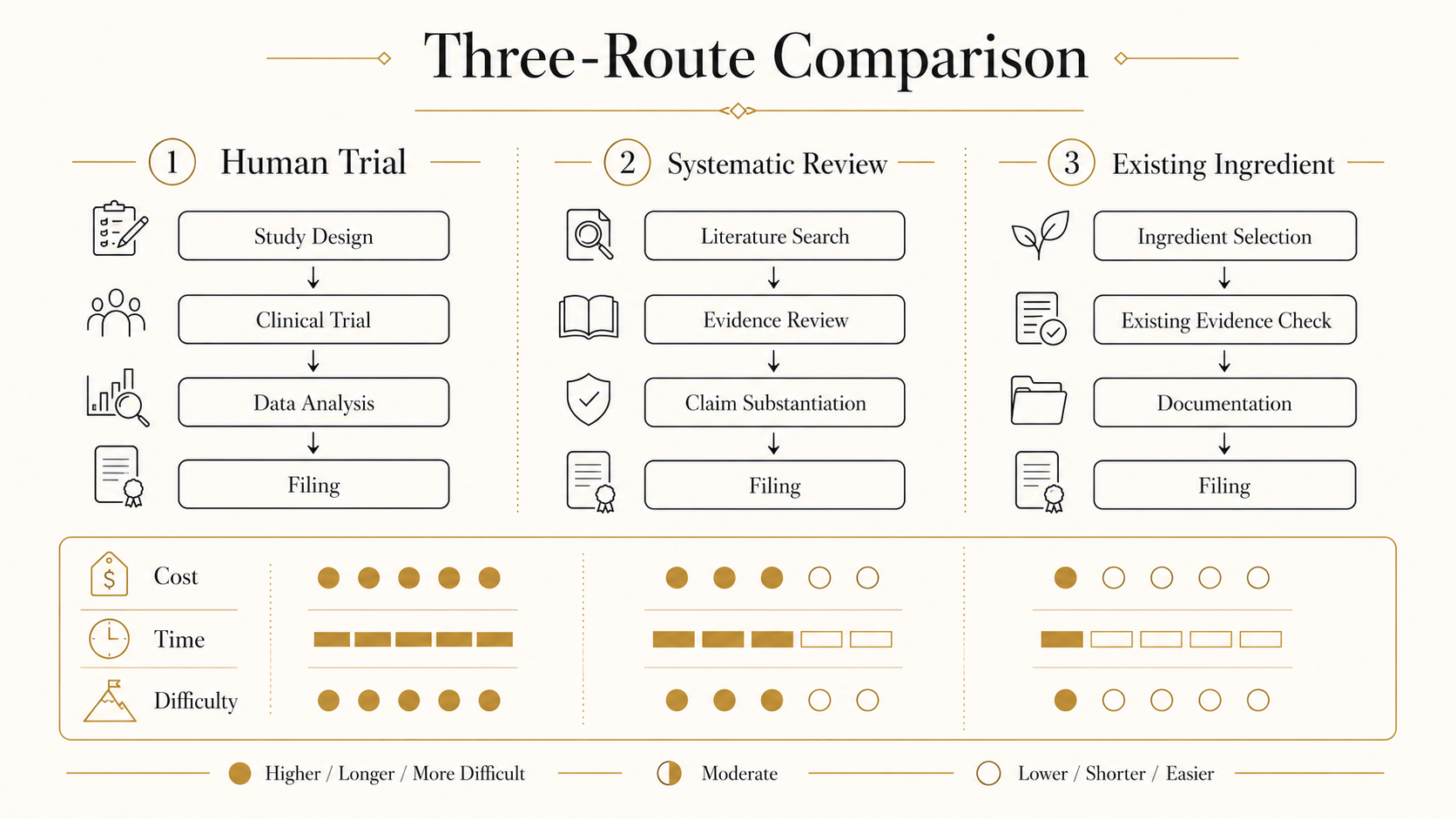
03研究レビュー(システマティックレビュー)
研究レビューは、PubMed・医中誌・JDream III等のデータベースから PRISMA 準拠 で文献を網羅的に収集し、ヒト介入試験の質的評価を行う作業です。専門的な統計知識と論文読解力が必要で、外部委託先と二人三脚で進めるのが一般的。
- 検索式の構築(PICO 設計)
- データベース検索・重複除外
- 論文スクリーニング(一次・二次)
- 論文の質評価(Cochrane Risk of Bias)
- 定性的・定量的統合(メタアナリシス)
- レビュー報告書の作成
採用論文の数だけでなく "質" が問われます。バイアスリスクが高い試験ばかりでは、機能性の根拠として弱いと判断されます。
04安全性評価
安全性は、(1) 既存情報による評価、(2) 摂取実績による評価、(3) 安全性試験の実施の3層で構築します。長年の食経験がある素材は (1)(2) で構成可能、新規素材は (3) の毒性試験データが必要。
05届出書の構成
届出書は様式I〜VIIで構成され、別紙資料として研究レビュー報告書、安全性評価書、製造工程フロー図、表示見本を添付。総ページ数は概ね 200〜400ページになります。

06提出と公表
届出は消費者庁の届出データベースへ電子提出。受理から 60日を経て差戻しがなければ公表され、表示開始可能になります。差戻しが入った場合は、コメントへの回答書を作成し再提出。慣れない初届出では2〜3往復が標準です。
「届出は1回で通すもの」と思わず、「2回往復する前提でスケジュールを引く」のが現場の鉄則。— 真鶴 薬事チーム
真鶴では原料選定から届出代行まで一貫して受託します。→ お問い合わせ
